Video Overlay Titlle
Video Overlay description

抗CLDN18抗体を用いると、主なアイソフォームであるCLDN18.1とCLDN18.2のいずれも検出します。ただし、下記の理由から、胃/GEJ癌組織において染色が認められた場合には、CLDN18.2が発現していると判断できます2,3。
正確な判定結果を得るためには、適切な検体の取り扱いと処理が不可欠です1,4。
Takeshi Kuwata, MD, PhD

使用する体外診断用医薬品等の電子化された添付文書の記載に従って処理すること4。
検体は採取後速やかに固定すること4。
ベンタナOptiView CLDN18(43-14A)の固定条件は下記の通りです4。
固定液は10%中性緩衝ホルマリンを使用し、固定には検体の15~20倍量を用いること。
10%中性緩衝ホルマリンを使用し、15~25℃で6~48時間固定すること。
判定結果に影響を及ぼすアーチファクトを最小にするために、プレアナリシス段階のさまざまな要因を適切に処理することが大切です。
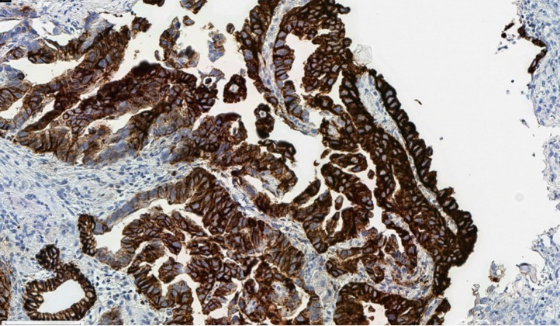
固定不良により細胞質まで染まり、
膜染色性の評価に影響が及んだ検体例
通常の処理を行ったホルマリン固定パラフィン包埋(FFPE)組織を使用すること。
CLDN18検査では、検体となる切片は4μmに薄切すること。
薄切後は速やかに染色を実施すること。


「切除不能進行・再発胃癌バイオマーカー検査の手引き(第2版)」では、適切なタイミングでバイオマーカー検査を実施し、治療方針を決定すべきとされています6。
また、治療開始までの時間を短縮し、最適な治療薬の投与機会を逸しないために、CLDN18、HER2、MSI/MMR、PD-L1の4検査をすべて同時に実施することが推奨されています6。
バイオマーカーの同時検査を実施しない場合には、各検査の陰性が確認された段階で、逐次検査を実施するフローが必要となります。
Turn Around Timeが長くなり、治療開始が遅れたり、場合によっては検体の再取得が必要となるケースも考えられます。リスクを回避し、臨床医・患者双方にデメリットが生じないように、適切なバイオマーカー検査を意識すべきであると考えられます。
監修:国立がん研究センター東病院 遺伝子診療部門 部門長 桑田 健 先生


参考資料:1. Compton CC, et al.: Arch Pathol Lab Med. 2019; 143(11): 1346-1363. 2. Fassan M, et al.: Mod Pathol. 2024; 37(11): 100589.(本論文の著者に同社より助成金、コンサルティング料等を受領している者、アドバイザリーボードメンバーが含まれる) 3. Sahin U, et al.: Clin Cancer Res. 2008; 14(23): 7624-7634.(本論文の著者にGanymed社の社員、アドバイザリーボードメンバーが含まれる) 4. ベンタナOptiView CLDN18(43-14A)電子添文 5. Pellino A, et al.: J Pers Med. 2021; 11(11): 1095.(本試験はアステラス製薬の支援により実施された。本論文の著者に同社より助成金、コンサルティング料等を受領している者が含まれる) 6. 日本胃癌学会編 : 切除不能進行・再発胃癌バイオマーカー検査の手引き 第2版