Video Description Title
Video Description description
CLDN18.1
主に肺の正常組織および肺癌組織に存在します9,10。
CLDN18.2
主に胃の正常組織に存在し、癌化後も発現が維持されます9,10。
Matteo Fassan, MD, PhD
正常組織における局在
癌化後の発現維持と露出
転移巣における発現維持
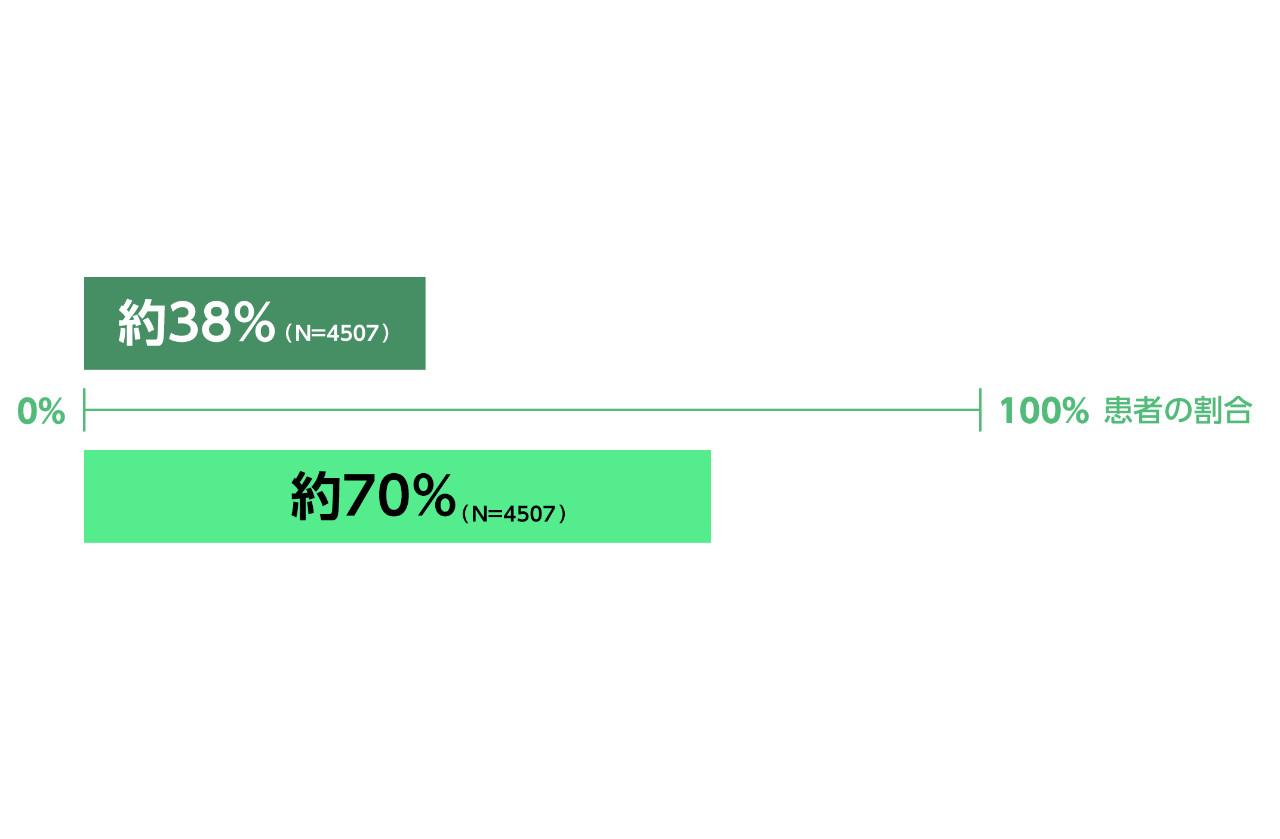
治癒切除不能な進行・再発の胃癌(GEJ腺癌を含む)患者4507例を対象とした2つの国際共同第Ⅲ相試験では、スクリーニングが実施され、IHC検査で評価可能であった患者の約38%*1がCLDN18.2陽性*2でした2。
*1:VENTANA CLDN18(43-14A)RxDx Assayを用いたIHC法による中央判定
*2:75%以上の腫瘍細胞において、細胞膜がCLDN18のIHC染色で中程度(2+)~強度(3+)の染色を示す。
国際共同第Ⅲ相試験:SPOTLIGHT試験
(海外データを含む)[検証試験]
【試験概要】CLDN18.2陽性かつHER2陰性の治癒切除不能な進行・再発の胃癌(GEJ腺癌を含む)患者565例を対象に、1:1の割合でゾルベツキシマブ+mFOLFOX6群およびプラセボ+mFOLFOX6群にランダムに割り付けた。なお、ホリナートはmFOLFOX6療法では国内承認外である。
国際共同第Ⅲ相試験:GLOW試験
(海外データを含む)[検証試験]
【試験概要】CLDN18.2陽性かつHER2陰性の治癒切除不能な進行・再発の胃癌(GEJ腺癌を含む)患者507例を対象に、1:1の割合でゾルベツキシマブ+CAPOX群およびプラセボ+CAPOX群にランダムに割り付けた。
*3つの単施設の研究データ。研究1はイタリアのPaduaで実施された進行胃癌患者 (280例)およびGEJ癌患者(70例)を対象とした研究16、研究2は日本人進行胃/GEJ腺癌患者408例を対象とした研究19、研究3はMD Anderson Cancer Center (MDACC)で実施された進行胃/GEJ腺癌患者304例を対象とした研究20でした。

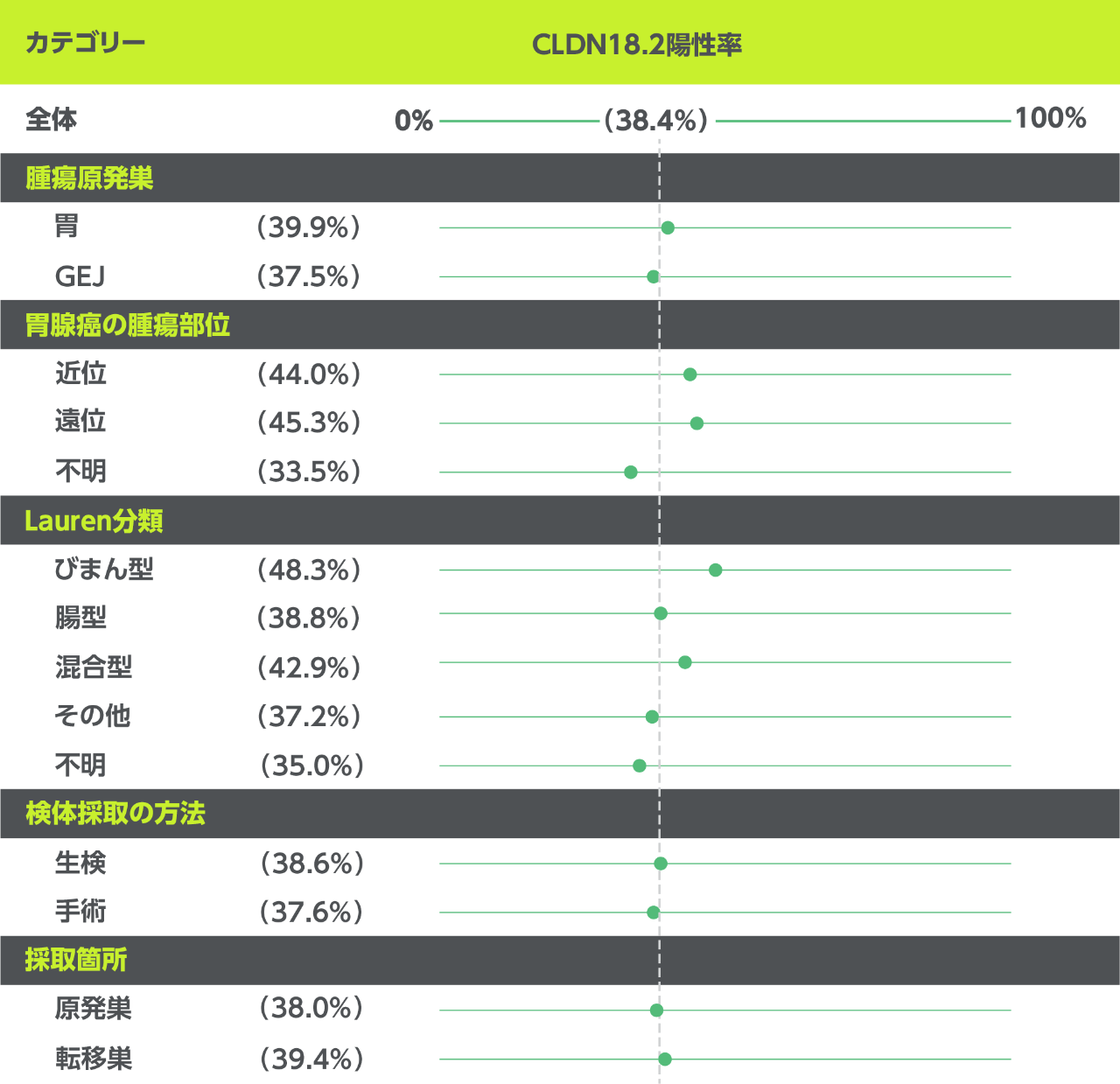
2つの国際共同第Ⅲ相試験においてスクリーニングを受けた患者における疾患特性および腫瘍検体特性別のCLDN18.2陽性率(4507例)2
胃/GEJ腺癌患者のデータから、原発巣と転移巣のCLDN18.2発現状況は一致したと報告されています17, 23, 24。
リンパ節転移:原発性胃/GEJ腺癌患者523例を対象とした研究によると、同一患者における原発巣と同時性リンパ節転移巣(135組)のCLDN18.2発現状況の一致率は下記の通りでした。

腹膜転移:2つの研究によると、原発巣と腹膜転移巣のCLDN18.2発現状況の一致率は下記の通りでした23, 24。


HER2などほかのバイオマーカーと同様に、胃/GEJ腺癌におけるCLDN18.2の発現には腫瘍内不均一性があると考えられていることから、検体採取時はこの点を考慮する必要があります17, 25。
原発巣と転移巣のCLDN18.2発現状況の一致率を報告した研究では、腫瘍内不均一性が下記の割合で認められました17。
原発性胃癌
原発性GEJ癌
リンパ節転移巣

参考資料:1. Fassan M, et al.: Mod Pathol. 2024; 37(11): 100589.(本論文の著者に同社より助成金、コンサルティング料等を受領している者、アドバイザリーボードメンバーが含まれる) 2. Shitara K, et al.: Gastric Cancer. 2024; 27(5): 1058-1068.(本試験はアステラス製薬の支援により実施された。本論文の著者に同社より助成金、コンサルティング料等を受領している者、同社の社員が含まれる) 3. Shah MA, et al.: Nat Med. 2023; 29(8): 2133-2141.(本試験はアステラス製薬の支援により実施された。本論文の著者に同社より助成金、コンサルティング料等を受領している者、同社の社員が含まれる) 4. Brezden-Masley C, et al.: Curr Oncol. 2024; 31(12): 7770-7786. 5. Wang FH, et al.: Cancer Commun (Lond). 2024; 44(1): 127-172. 6. Lordick F, et al.: Onkopedia. German S3 guideline on gastric cancer 2025 update. https://www.onkopedia.com/en/onkopedia/guidelines/gastric-cancer/@@guideline/html/index.html(2025年12月閲覧) 7. Alsina Maqueda M, et al.: Clin Transl Oncol. 2025; 27(9): 3580-3594. 8. ESMO. Gastric Cancer Living Guidelines. Version 1.4. September 2024. https://www.esmo.org/guidelines/living-guidelines/esmo-living-guideline-gastric-cancer/diagnosis-pathology-and-molecular-biology.(2025年12月閲覧) 9. Sahin U, et al.: Clin Cancer Res. 2008; 14(23): 7624-7634.(本論文の著者にGanymed社の社員、アドバイザリーボードメンバーが含まれる) 10. Niimi T, et al.: Mol Cell Biol. 2001; 21(21): 7380-7390. 11. Tsukita S, et al.: Trends Biochem Sci. 2019; 44(2): 141-152. 12. Hu YJ, et al.: Mol Biol Rep. 2013; 40(11): 6123-6142. 13. 日本胃癌学会編 : 切除不能進行・再発胃癌バイオマーカー検査の手引き 第2版 14. Sahin U, et al.: Eur J Cancer. 2018; 100: 17-26.(本試験はGanymed社の支援により実施された。本論文の著者に同社よりコンサルティング料を受領している者、同社の社員が含まれる) 15. Lamouille S, et al.: Nat Rev Mol Cell Biol. 2014; 15(3): 178-196. 16. Pellino A, et al.: J Pers Med. 2021; 11(11): 1095.(本試験はアステラス製薬の支援により実施された。本論文の著者に同社より助成金、コンサルティング料等を受領している者が含まれる) 17. Coati I, et al.: Br J Cancer. 2019; 121(3): 257-263. 18. Rohde C, et al.: Jpn J Clin Oncol. 2019; 49(9): 870-876.(本試験はGanymed社の支援により実施された。本論文の著者に同社の社員が含まれる) 19. Kubota Y, et al.: ESMO Open. 2023; 8(1): 100762.(本試験はアステラス製薬の支援により実施された) 20. Waters R, et al.: JCO Precis Oncol. 2024; 8: e2300543.(本試験はアステラス製薬の支援により実施された。本論文の著者に同社より助成金、コンサルティング料等を受領している者、同社の社員が含まれる) 21. 国立がん研究センター : がん情報サービス「がん統計」(全国がん登録 罹患数・率 報告). 2021 22. 国立がん研究センター : がん診療連携拠点病院等院内がん登録 2014-2015年 5年生存率集計 報告書, 2023 23. Angerilli V, et al.: Gastric Cancer. 2025; 28(4): 569-578. 24. Ogawa H, et al.: Gastric Cancer. 2024; 27(4): 802-810. 25. Grillo F, et al.: World J Gastroenterol. 2016; 22(26): 5879-5887.